
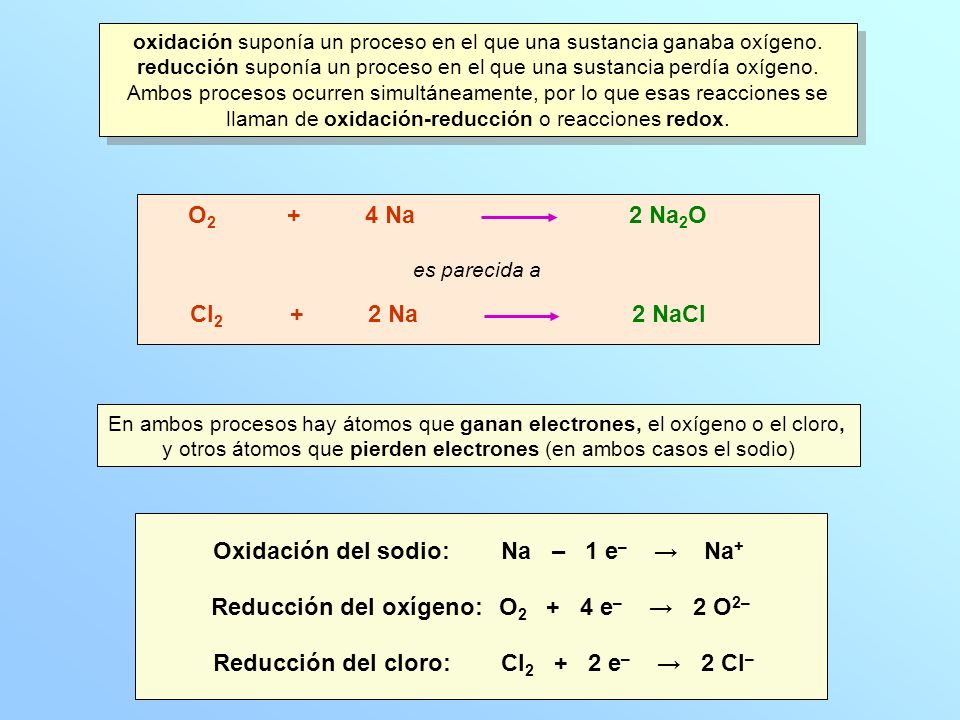
Ejemplo de reacción de oxidación-reducción
Las reacciones de oxidación-reducción, también conocidas como reacciones redox, son aquellas en las que se produce una transferencia de electrones entre los reactivos. Son procesos muy comunes en la Eemplo y desempeñan un papel fundamental en muchas reacciones químicas y biológicas.
Un ejemplo clásico de una reacción redox es la combustión.
Combustión del metano
Un ejemplo representativo de una reacción de oxidación-reducción es la combustión del metano (CH4).
En esta reacción, el metano reacciona con oxígeno (O2) para formar dióxido de carbono (CO2) y agua (H2O). La ecuación química de esta reacción es la siguiente:
CH4 + 2O2 → CO2 oxidaciob- 2H2O
En esta reacción, el metano se oxida perdiendo hidrógeno y ganando oxígeno, y el oxígeno se reduce ganando electrones. El metano es el agente reductor, ya que permite que otra especie química gane electrones, mientras que el oxígeno es el agente oxidante, ya que provoca la oxidación del metano.
Balanceo de la ecuación química
Para asegurarnos de que la ecuación química esté correctamente balanceada, es necesario igualar el número de átomos de cada elemento en ambos lados de la ecuación.

En el caso de la combustión del metano, podemos ver que hay un átomo de carbono en el lado izquierdo de la ecuación y un átomo de carbono en el lado derecho. Sin embargo, hay cuatro átomos de hidrógeno en el lado izquierdo y solo dos en el lado derecho. Para balancear la ecuación, necesitamos duplicar la cantidad de agua en el lado derecho:
CH4 + 2O2 → CO2 + 4H2O
Ahora, la ecuación química está balanceada, con igual raeccion de átomos de cada elemento en ambos lados.
Esto es esencial para que se conserve la ley de conservación de la masa en una reacción química.
Importancia de las reacciones de oxidación-reducción
Las reacciones de oxidación-reducción son de gran importancia en la vida cotidiana y en numerosos procesos industriales.
Por ejemplo, la respiración celular, que es el proceso mediante el cual las células obtienen energía, es una reacción redox. También, la carga y descarga de una batería se basa en reacciones redox, al igual que deaccion reacciones de síntesis y descomposición en la industria química.
En resumen, las reacciones de oxidación-reducción son procesos fundamentales en la química y desempeñan un papel crucial en diversas aplicaciones.
La combustión del metano es un ejemplo ilustrativo de una reacción redox, donde ocurre una transferencia de electrones entre los reactivos.
Su balanceo adecuado es esencial para cumplir con la ley de conservación de la masa.







